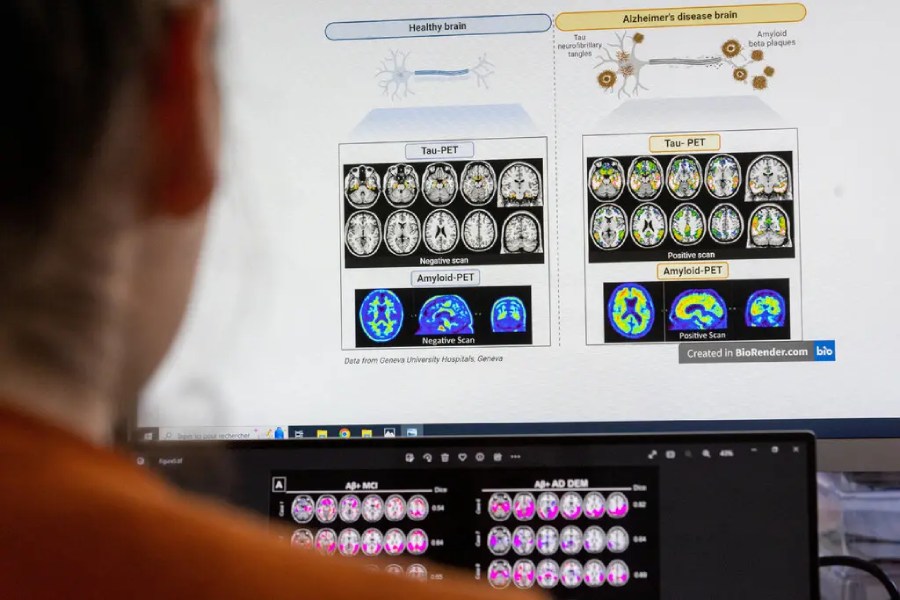
Агентство зазнало критики за те, що схвалило препарат Адугельм, не маючи чітких доказів того, що він діє
Адміністрація США з питань харчових продуктів і медикаментів схвалила перший за останні десятиліття новий препарат від хвороби Альцгеймера через заперечення статистичних агентств, які заявили, що недостатньо доказів, що підтверджують схвалення, згідно із нещодавно опублікованими внутрішніми записками.

- У внутрішніх записках, опублікованих у вівторок, представники FDA обговорили, чи слід схвалювати препарат від Biogen Inc. на ринку.
Зрештою, найвищі посадові особи вирішили, що докази, які свідчать про те, що препарат діяв, хоча і безрезультатні, були достатньо вагомими, щоб дозволити лікарям і пацієнтам самостійно вирішити, чи приймати його, згідно з записками.
«Отже, FDA стикається з ситуацією, коли наявні докази щодо клінічних кінцевих точок не вистачають того, що нам потрібно для стандартного затвердження адуканумабу», — написав Пітер Штейн, директор офісу FDA щодо нових препаратів, у записці, де підтримка для затвердження. «У той же час пацієнти з [хворобою Альцгеймера] мають серйозне, прогресуюче, в кінцевому підсумку смертельне захворювання, і відчайдушно потребують лікування».
FDA оприлюднила свої внутрішні обговорення, оскільки вона стикається з критикою з боку деяких лікарів та вчених через схвалення препарату, який називається Aduhelm, 7 червня.
Критики заявляють, що FDA ігнорує наукові стандарти, до яких вони зазвичай належать виробникам ліків, і може спонукати федеральний уряд витратити мільярди доларів на ліки, які можуть не працювати.
«Хоча я повністю підтримую нещодавнє рішення Центру затвердити терапію, я визнаю, що щодо цього рішення існують різні думки, в тому числі в рамках FDA, і, ймовірно, і надалі будуть виникати питання щодо нашого процесу перевірки та даних, які ми вважали на підтримку схвалення », — сказала виконуюча обов’язки комісара FDA Джанет Вудкок.
Зрештою, досвідчена група рецензентів з FDA дійшла висновку, що є достатньо доказів для схвалення терапії Альцгеймера за прискореним шляхом схвалення.
Прихильники заявляють, що рішення FDA забезпечує порятунок пацієнтам, яким бракувало будь-яких ліків, що обіцяють уповільнити прогресування хвороби Альцгеймера, і що це рішення може стимулювати розробку нових, кращих ліків.
Агентство зазвичай видає документи про затвердження після прийняття рішення, хоча, як правило, не так швидко, як цього разу. 83 сторінки пам’яток, здається, є частиною обговорень FDA, в основному відображаючи обмін вищими посадовими особами.
- Трістан Массі, рецензент біостатистики з FDA, «не згоден з тим, що сукупність даних забезпечує достатні докази, що підтверджують ефективність адуканумабу при хворобі Альцгеймера, і не рекомендує затверджувати», — вказується в одному з внутрішніх документів.
Патріція Каваццоні, найвища посадова особа з оцінки лікарських засобів FDA, написала в іншій записці, що Управління з біостатистики лікарських засобів агентства «надало документацію для рекомендації, згідно з якою в заявці не було надано суттєвих доказів ефективності».
Повний окремий аналіз цього відомства не був включений до матеріалів, опублікованих у вівторок, але деякі з них були.
Незважаючи на заперечення, доктор Каваццоні написав, що Біоген відповідав вимогам щодо «прискореного затвердження», типу регуляторного дозволу, який дозволяє лікарському засобу продаватися, навіть коли залишається невизначеність щодо його клінічної вигоди, якщо це заповнює незадоволену потребу в серйозне захворювання і впливає на біологічні ознаки захворювання.
Доктор Каваццоні писав, що Адугельм відповідав цьому стандарту через його ефект зменшення липкої речовини під назвою амілоїд, яка «з достатньою ймовірністю передбачає клінічну користь».
Деякі лікарі та вчені кажуть, що націлювання на амілоїдні бляшки не доведено сповільнювати хворобу Альцгеймера. Деякі члени групи радників, які рекомендували FDA відхилити препарат, звільнилися з комітету, посилаючись на схвалення агентства.
Біоген вказав ціну Aduhelm у 56 000 доларів на рік, а пацієнти та Medicare також можуть зіткнутися з випробуванням.
Близько шести мільйонів американців страждають на хворобу Альцгеймера — прогресуючий стан, який позбавляє людей спогадів та когнітивних здібностей. Біоген заявив, що ці два мільйони з них можуть отримати користь від ліків.
Що ви можете зробити, щоб знизити ризик розвитку хвороби Альцгеймера?